 新闻资讯
新闻资讯

一张印有FDA标识的认证证书背后,是跨越太平洋的技术长征,更是中国高端医疗装备叩开全球最严苛市场大门的重量级通行证。

全球医疗市场的“黄金标准”
中国智造的“终极试炼”
美国食品药品监督管理局(FDA)认证被公认为全球医疗器械准入的最高门槛,其审核体系以风险等级为核心,将产品分为三类:
I类器械(低风险):如绷带、体温计,仅需基础监管;
II类器械(中风险):如内窥镜、监护仪,需提交510(k)申请,证明与已上市产品“实质等效”,平均审核周期90天;
III类器械(高风险):如心脏起搏器,需通过PMA(上市前批准),提交完整临床试验数据,费用高达数十万美元。
此次海斯凯尔的共聚焦激光显微内镜CelTouch®以II类器械身份获批,标志着产品技术安全性和有效性已达到国际先进水平,也是国内同类产品中优先获得海外的市场认证资格。
从“看得见”到“看得清”
重新定义活体显微诊断
共聚焦激光显微内镜CelTouch®是一项突破性的超高分辨率显微成像技术,能够将体内组织细胞放大至1000倍,实现微米级分辨率成像,为临床提供“在体实时光学病理”图像。120FPS高频运动级成像,聚焦深度达120μm,分辨率精确至1μm,自动校准,稳定输出。同时搭载AI辅助诊断系统、自体荧光信号增强系统等强大功能,不仅能即时判断病变的良恶性质,大幅提高早期病变检出率、减少取样误差和漏诊率,还极大缩短了诊断时间,提升了治疗效率,真正实现“所见即所得”的可视化精准操作。广泛应用于消化道、呼吸、泌尿等领域的早癌筛查。未来,或将逐步推动临床诊疗从传统组织病理向光学病理的转型。
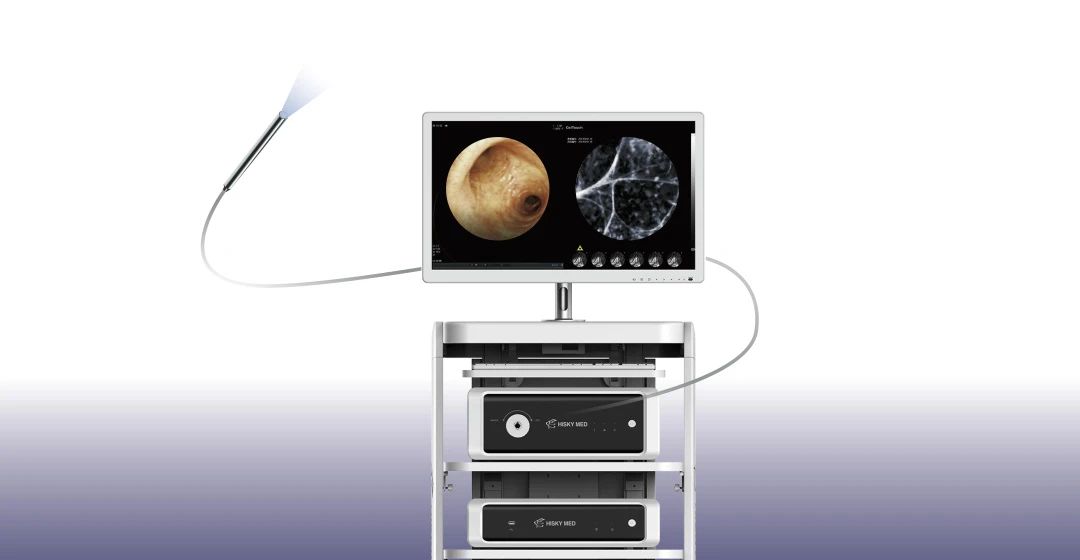
中国智造照亮海外市场
全球内镜版图正在重构。当AI结合虚拟染色内镜和超高倍内镜,进行黏膜炎症程度的自动量化时;当治疗型内镜完成光动力治疗时;当肠镜筛查纳入欧美医保体系时;海斯凯尔带着CelTouch®冲进了技术跃迁的齿轮,价格已不再是最大杀器,国产自研的创新技术,高效的辅助诊断系统和稳定的临床应用才是真正密钥。
通过FDA认证不是终点,而是中国技术参与全球健康治理的新起点!中国医疗器械的全球化叙事已悄然改写——从“成本优势”到技术话语权,从“代工制造”到标准制定者,从“单点突破”到系统性创新。这每一步,都是中国医疗技术从业人员的足迹和坚持。
当中国智造的显微之光穿透人体组织的迷雾时,照亮的何尝不是人类对抗疾病的共同疆域。精密探针在黏膜层游走的轨迹,正在刻写属于中国创新的生命密码,细胞级精度的星光之下,映照着智能医疗的星辰大海。
海斯凯尔
海斯凯尔医学技术源于清华大学,以“普及高端科技,守护大众健康”为己任,致力于成为医疗创新诊疗技术的领军企业,为人类健康做出卓越贡献。旗下拥有多个自主研发品牌,包括iLivTouch®无创肝脏检测系统、CelTouch®共聚焦激光显微内镜、EQTouch®高端超声科研平台以及乳腺疾病诊治解决方案,可应用于肝脏、消化、体检、呼吸、乳腺、泌尿、外科等领域的无创筛查、诊断及诊后管理。
海斯凯尔研发实力雄厚,先后参与了国家十二五科技支撑计划、国家十三五科技重大专项、北京市自然科学基金重点项目等多个国家级或省部级科技项目,累计申请国内外专利600余件,在先进光学系统、先进声学系统和智能成像领域达到国际先进水平。先后获得了包括国家专精特新“小巨人”企业称号、黄家驷生物医学工程奖、华夏医学科技奖、中华医学科技奖、中国专利优秀奖以及多个省市的科学技术/发明奖在内的诸多荣誉。
海斯凯尔在北京、山东、江苏等地分别建有基地,业务网络覆盖全国。与此同时,海斯凯尔获得了美国FDA、欧盟CE、日本PMDA、澳大利亚TGA、韩国KFDA、俄罗斯RZN等海外市场认证,产品已销往全球近70个国家或地区,服务于海内外数千万患者。